Hukum Hess menyatakan jumlah panas yang terlibat dalam suatu reaksi kimia hanya dipengaruhi oleh keadaan awal dan akhir. Selain itu, dalam Hukum Hess juga menegaskan bahwa jumlah panas yang terlibat dalam suatu reaksi kimia tidak bergantung terhadap jalannya reaksi. Dua pernyataan tersebut termuat dalam Bunyi Hukum Hess yaitu “Entalpi reaksi tidak bergantung pada jalannya reaksi melainkan bergantung pada hasil akhir reaksi”.
Entalpi (H) adalah banyaknya kalor yang dimiliki sistem pada tekanan tetap. Dari bunyi hukum Hess dapat diperoleh/ disimpulkan beberapa pernyataan yang benar tentang perubahan entalpi sesuai Hukum Hess.
Apa saja pernyataan yang benar tentang perubahan entalpi berdasarkan Hukum Hess? Bagaimana penerapan Hukum Hess? Sobat idschool dapat mencari tahu cara menentukan atau menyimpulkan pernyataan yang benar tentang perubahan entalpi sesuai Hukum Hess melalui ulasan di bawah.
Hukum Hess
Teori dalam Hukum Hess disampaikan oleh seorang ahli kimia bernama Henry Hess. Teori yang disampaikannya menerangkan bahwa perubahan entalpi tidak bergantung pada jalannya reaksi atau tahapan reaksi. Namun, perubahan entalpi bergantung pada keadaan awal dan akhir reaksi.
Keadaan awal dalam Hukum Hess menunjuk pada keadaan reaktan. Sementara keadaan akhir menunjuk pada keadaan produk. Dalam penulisan reaksi kimia, posisi reaktan berada di sebelah kiri produk yang dipisahkan tanda panah. Misalnya pada reaksi C (s) + O2 (g) → CO2 (g), didapat C + O2 adalah reaktan dan CO2 adalah produk.

Baca Juga: Hubungan Rumus q Reaksi dan Perubahan Entalpi (ΔH)
Hukum Hess dapat digunakan untuk menghitung perubahan entalpi (ΔH). Dalam perhitungan perubahan entalpi dengan Hukum Hess memperhatikan aturan-aturan berikut.
- Reaksi yang dibalik akan merubah tanda perubahan entalpi
Contoh:
A + B → C ΔH = +n kJ
C → A + B ΔH = ‒n kJ
- Perubahan koefisien akan mempengaruhi perubahan entalpi, jika reaksi dikalikan dengan suatu faktor maka perubahan entalpi juga perlu dikalikan dengan faktor yang sama.
Contoh:
A + ½B → C ΔH = +m kJ
2A + B → 2C ΔH = +2m kJ
½A + ¼B → ½C ΔH = +½m kJ
Baca Juga: 4 Cara yang Dapat Digunakan untuk Menghitung Perubahan Entalpi (ΔH)
Contoh Penggunaan Hukum Hess
Perhatikan contoh bagaimana penggunaan Hukum Hess untuk menentukan perubahan entalpi pada reaksi C (s) + 2H2 (g) → CH4 (g) melalui soal berikut.
Diketahui perubahan entalpi dari reaksi-reaksi berikut.
- C (s) + O2 (g) → CO2 (g) ΔH = ‒393,5 kJ
- 2H2 (g) + O2 (g) → 2H2O (l) ΔH = ‒571,6 kJ
- CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (l) ΔH = ‒890,4 kJ
Penyelesaian:
Untuk menentukan perubahan entalpi dari reaksi C (s) + 2H2 (g) → CH4 (g) perlu menyesuaikan posisi reaktan dan produk dari reaksi-reaksi yang sudah diketahui perubahan entalpinya.
Dari reaksi C (s) + 2H2 (g) → CH4 (g) didapat reaktan: C (s) + 2H2 (g) dan produk: CH4 (g). Sehingga reaksi yang memuat C yaitu C (s) + O2 (g) → CO2 (g) tetap, selain itu reaksi yang memuat H2 yaitu 2H2 (g) + O2 (g) → 2H2O (l) juga tetap.
Sementara untuk reaksi CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (l) perlu dibalik karena posisi CH4 pada reaksi yang ditanyakan adalah produk. Sedangkan posisi CH4 pada reaksi yang diketahui merupakan reaktan.
Selanjutnya, pernyataan yang benar tentang perubahan entalpi sesuai Hukum Hess dapat dihitung dengan menjumlahkan perubahan entalpi dari reaksi-reaksi yang telah disesuaikan. Cara menghitung perubahan entalpi untuk reaksi C (s) + 2H2 (g) → CH4 (g) sesuai pada cara penyelesaian berikut.

Jadi, perubahan entalpi reaksi: C (s) + 2H2 (g) → CH4 (g) adalah ‒74,7 kJ.
Baca Juga: Karakteristik Rekasi Endoterm dan Eksoterm pada Termokima
Contoh Soal dan Pembahasan
Beberapa contoh soal pernyataan yang benar tentang perubahan entalpi di bawah dapat sobat idschool gunakan untuk menambah pemahaman bahasan di atas. Setiap contoh soal yang diberikan dilengkapi dengan pembahasan cara menyimpulkan pernyataan yang benar tentang perubahan entalpi sesuai Hukum Hess. Sobat idschool dapat menggunakan pembahasan tersebut sebagai tolak ukur keberhasilan mengerjakan soal. Selamat Berlatih!
Contoh 1 – Soal Pernyataan yang Benar Tentang Perubahan Entalpi Sesuai Hukum Hess
Pernyataan yang benar di bawah ini mengenai hukum Hess adalah ….
(A) Entalpi hanya bergantung pada keadaan awal reaksi
(B) Entalpi hanya bergantung pada keadaan akhir reaksi
(C) Entalpi hanya bergantung pada keadaan awal dan akhir reaksi, maka perubahan entalpi tidak bergantung pada jalannya reaksi (proses)
(D) Entalpi bergantung pada keadaan awal dan akhir reaksi, dan juga bergantung pada jalannya reaksi (proses)
(E) Entalpi tidak bergantung pada keadaan awal dan akhir reaksi, tetapi hanya bergantung pada jalannya reaksi (proses)
Pembahasan:
Pernyataan yang benar mengenai hukum Hess dapat disimpulkan dari bunyi Hukum Hess yang menyatakan bahwa entalpi reaksi tidak bergantung pada jalannya reaksi melainkan bergantung pada hasil akhir reaksi.
Jadi, pernuataan yang benar di bawah ini mengenai Hukum Hess adalah Entalpi hanya bergantung pada keadaan awal dan akhir reaksi, maka perubahan entalpi tidak bergantung pada jalannya reaksi (proses).
Jawaban: C
Contoh 2 – Pernyataan yang Benar Tentang Perubahan Entalpi Sesuai Hukum Hess
Diketahui diagram Hukum Hess sebagai berikut!

Pernyataan yang benar tentang perubahan entalpi sesuai Hukum Hess untuk diagram di atas adalah ….
A. ΔH4 = ΔH1 + ΔH2 + ΔH3
B. ΔH1 + ΔH3 = ΔH4 + ΔH2
C. ΔH3 = ΔH1 + ΔH2 ‒ ΔH4
D. ΔH2 = ΔH1 + ΔH4 + ΔH3
E. ΔH2 = ΔH1 + ΔH3 ‒ ΔH4
Pembahasan:
Dari gambar diagram Hukum Hess dapat diketahui bahwa dari A menjadi C dapat melalui tahapan A → B → C atau A → D → C.
Perubahan entalpi untuk reaksi A → C melalui tahapan A → B → C = ΔH4 + ΔH3. Sedangkan perubahan entalpi untuk reaksi A → C melalui tahapan A → D → C = ΔH1 + ΔH2. Berdasarkan Hukum Hess perubahan entalpi hanya bergantung pada kondisi awal dan akhir, dan tidak bergantung dari tahapannya.
Sehingga dapat diperoleh persamaan:
ΔH4 + ΔH3 = ΔH1 + ΔH2
ΔH3 = ΔH1 + ΔH2 ‒ ΔH4
Jadi, pernyataan yang benar tentang perubahan entalpi sesuai Hukum Hess untuk diagram yang diberikan adalah ΔH3 = ΔH1 + ΔH2 ‒ ΔH4.
Jawaban: C
Contoh 3 – Pernyataan yang Benar Tentang Perubahan Entalpi
Beberapa pernyataan yang benar tentang perubahan entalpi terdapat pada kalimat-kalimat berikut, kecuali ….
(A) Perubahan entalpi merupakan perubahan kalor pada tekanan tetap.
(B) Nilai perubahan entalpi tergantung pada jumlah zat, suhu, dan tekanan.
(C) Nilai perubahan entalpi dipengaruhi oleh jalannya reaksi.
(D) Nilai perubahan entalpi standar diukur pada 298 oK dan 1 atm.
(E) Nilai perubahan entalpi dapat ditentukan dengan cara kalorimeter.
Pembahasan:
Dari bunyi Hukum Hess jelas menerangkan bahwa perubahan entalpi reaksi tidak bergantung dari tahapan atau jalannya reaksi. Perubahan entalpi reaksi bergantung dari kondisi awal (reaktan) dan akhir (produk) reaksi.
Jadi, semua pernyataan yang benar tentang perubahan entalpi terdapat pada pilihan kecuali Nilai perubahan entalpi dipengaruhi oleh jalannya reaksi.
Jawaban: C
Contoh 4 – Pernyataan yang Benar Tentang Perubahan Entalpi
Pernyataan:
(i) Kalor berpindah dari sistem ke lingkungan
(ii) Kalor berpindah dari lingkungan ke sistem
(iii) Persamaan termokimia: CaO (s) + CO2 (g) → CaCO3 (s) ΔH = ‒a kJ
(iv) Untuk menghasilkan 0,5 mol CaCO3 sistem melepaskan energi sebesar 2a kJ
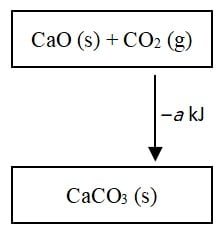
Pernyataan yang benar mengenai diagram tingkat energi di atas ditunjukkan oleh angka ….
A. (i) dan (iii)
B. (i) dan (iv)
C. (ii) dan (iii)
D. (ii) dan (iv)
E. (iii) dan (iv)
Pembahasan:
Dari diagram yang diberikan dapat diketahui bahwa reaksi CaO (s) + CO2 (g) → CaCO3 (s) melepaskan a kJ karena nilai ΔH < 0 (negatif). Reaksi yang memiliki nilai perubahan entalpi (ΔH) negatif merupakan reaksi eksoterm. Pada reaksi eksoterm terjadi perpindahan kalor dari sistem ke lingkungan. Sehingga pernyataan nomor (i) benar.
Dari gambar diketahui bahwa pembentukan CaCO3 dari CaO dan CO2 melepaskan energi sebanyak a kJ. Dalam reaksi termokimia dapat dituliskan Persamaan termokimia: CaO (s) + CO2 (g) → CaCO3 (s) ΔH = ‒a kJ (pernyataan (iii) benar).
Jadi, pernyataan yang benar mengenai perubahan entalpi sesuai diagram ditunjukkan oleh angka (ii) dan (iii).
Jawaban: C
Contoh 5 – Pernyataan yang Benar Tentang Perubahan Entalpi
Perhatikan diagram pembentukan gas ML3 berikut!
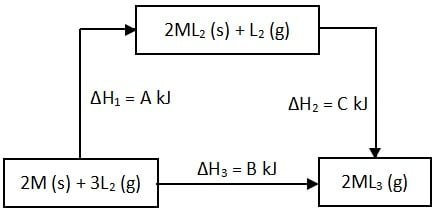
Pernyataan yang benar tentang perubahan entalpi menurut Hukum Hess sesuai diagram di atas adalah ….
A. penguraian 1 mol ML2 adalah ½C
B. perubahan entalpi untuk pembentukan 1 mol ML3 adalah ½B
C. hubungan ketiga energi tersebut adalah C = A ‒ B
D. pembentukan ML2 membutuhkan energi yang lebih besar daripada pembentukan ML3
E. hubungan ketiga energi tersebut adalah C = A + B
Pembahasan:
Sesuai bunyi Hukum Hess, dari diaragm dapat diperoleh persamaan bahwa H3 = H1 + H2 atau B = A + C. Reaksi-reaksi pada diagram jika dituliskan dalam persamaan termokimia sesuai dengan tiga reaksi berikut.
- 2M (s) + 3L2 (g) → 2ML2 (g) + L2 (g) ΔH1 = A kJ
- 2ML2 (g) + L2 (g) → 2ML3 (g) ΔH = C kJ
- 2M (s) + 3L2 (g) → 2ML3 (g) ΔH = B kJ
Dari reaksi ketiga dapat diketahui bahwa perubahan entalpi untuk pembentukan 1 mol ML3 dilakukan dengan mengalikan ½. Sehingga diperoleh persamaan ½ [2M (s) + 3L2 (g) → 2ML3 (g) ΔH = B kJ] atau M (s) + 3/2L2 (g) → ML3 (g) ΔH = ½B kJ.
Jadi, pernyataan yang benar dari diagram menurut Hukum Hess adalah perubahan entalpi untuk pembentukan 1 mol ML3 adalah ½B.
Jawaban: B
Demikianlah tadi ulasan apa saja pernyataan yang benar tentang perubahan entapi sesuai Hukum Hess. Terima kasih sudah mengunjungi idschool(dot)net, semoga bermanfaat!
Baca Juga: [Praktikum Kimia] Menentukan ΔH dengan Kalorimeter
