John Dalton mengenalkan sebuah kesimpulan mengenai perbandingan massa unsur dalam senyawa yang disebut hukum perbandingan berganda. Kesimpulan tersebut berupa pernyataan mengenai apabila ada unsur-unsur yang membentuk dua/lebih senyawa yang massa salah satu unsurnya sama banyak maka massa unsur yang kedua berbanding sebagai bilangan bulat dan sederhana. Ingat kembali bahwa ikatan kimia dari dua unsur dapat membentuk lebih dari satu macam senyawa, misalnya unsur karbon (C) dan unsur oksigen (O) dapat membentuk karbon monoksida (CO) dan karbon dioksida (CO2).
Pada pembentukan senyawa dari karbon (C) dan oksigen (O) membentuk karbon monoksida (CO) dan karbon dioksida (CO2) . Jika jumlah karbon yang bereaksi pada masing – masing adalah 1 gram maka teramati bahwa pada karbon monoksida yang terbentuk akan terdapat 1,33 gram oksigen, sedangkan pada karbon dioksida terbentuk 2,66 gram oksigen. Perhatikan bahwa perbandingan massa oksigen adalah 1 : 2. Hasil perbandingan tersebut membentuk bilangan bulat sederhana dan kemudian akan disebut sebagai hukum perbandingan berganda.

Bagaimana bunyi hukum perbandingan ganda yang diperkenalkan oleh Dalton? Bagaimana contoh soal hukum perbandingan berganda? Simak selanjutnya ulasan materi hukum perbandingan berganda (hukum Dalton) yang akan diberikan melalui ulasan di bawah.
Bunyi Hukum Perbandingan Berganda
Dua unsur bergabung dan masing-masing menyumbangkan sejumlah atom tertentu untuk membentuk ikatan kimia. Komposisi unsur-unsur dengan ikatan kimia membentuk suatu senyawa dan dituliskan dalam rumus kimianya. Dari dua unsur dapat dibentuk beberapa senyawa dengan perbandingan berbeda-beda.
Sebagai contoh, belerang (S) dengan oksigen (O) dapat membentuk senyawa SO2 (sulfur dioksida) dan SO3 (sulfur trioksida), unsur hidrogen (H) dan oksigen (O) dapat dibentuk senyawa H2O (air) dan H2O2 (hidrogen peroksida), dan unsur karbon (C) dan oksigen (O) membentuk senyawa CO (karbon monoksida) dan CO2 (karbon dioksida).
Bagaimana percobaan yang dilakukan Dalton sehingga dapat menyimpulkan hukum perbandingan berganda?
John Dalton mengamati perbandingan unsur – unsur pada setiap senyawa membentuk pola keteraturan. Perhatikan contoh percobaan hukum perbandingan berganda yang diperkenalkan Dalton dengan perolehan data sebagai berikut.

Data hasil percobaan yang dilakukan John Dalton menunjukkan bahwa perbandingan massa oksigen yang terikat oleh karbon dengan massa yang sama yaitu 1 : 2.
Baca Juga: Ikatan Kimia – Ion, Kovalen, dan Logam
John Dalton menyelidiki perbandingan unsur-unsur tersebut pada setiap senyawa dan mendapatkan suatu pola keteraturan. Pola tersebut dinyatakan sebagai hukum perbandingan berganda atau hukum Dalton.
Bunyi hukum perbandingan ganda Dalton tersebut adalah apabila dua unsur dapat membentuk lebih dari satu senyawa, massa salah satu unsur tersebut tetap (sama) maka perbandingan massa unsur yang lain dalam senyawa-senyawa tersebut merupakan bilangan bulat dan sederhana.

Untuk menambah pemahaman sobat idschool mengenai penerapan hukum perbandingan berganda pada soal, simak contoh soal hukum perbandingan ganda yang akan diberikan berikut.
Baca Juga: Cara Menentukan Rumus Molekul Senyawa
Contoh Soal Hukum Perbandingan Berganda dan Pembahasan
Beberapa contoh soal dibawha dapat sobat idschool gunakan untuk menambah pemahaman bahasan di atas. Setiap contoh soal yang diberikan dilengkapi dengan pembahasannya. Sobat idschool dapat menggunakna pembahasan tersebut sebagai tolak ukur keberhasilan mengerjakan soal. Selamat Berlatih@
Contoh 1 – Soal Hukum Perbandingan Berganda
Sebuah senyawa A disusun oleh 63,6% unsur N dan 34,6% unsur O. dan senyawa B disusun oleh 46,7% unsur N dan 53,3% unsur O. Tunjukkan bahwa senyawa tersebut sesuai hukum perbandingan berganda dari Dalton dan tentukan rumus senyawa A tersebut!
Pembahasan:
- Menunjukkan senyawa A dan Senyawa B sesuai hukum perbandingan berganda Dalton
Untuk menunjukkan senyawa A sesuai hukum perbandingan berganda dalton, sobat idschool dapat menggunakan informasi persentase unsur yang digunakan. Sederhanakan bentuk perbandingan persentase menjadi bentuk yang paling sederhana.
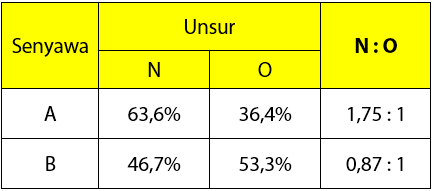
Perhitungan perbandingan:

- Menentukan rumus senyawa A:
Senyawa A (satu unsur O dan dua unsur N) ~ NO2
Senyawa B (satu unsur O dan satu unsur N) ~ NO
Baca Juga: 5 Hukum Kimia Dasar
Contoh 2 – Soal Hukum Perbandingan Berganda Dalton

Karbon dan oksigen dapat membentuk dua macam senyawa yaitu CO dan CO2. Jika kandungan karbon pada senyawa CO dan CO2 berturut-turut 42,85% dan 27,2%. Apakah data ini sesuai hukum Dalton?
Pembahasan:
Langkah pertama dalah menghitung perbandingan massa karbon dan massa oksigen.
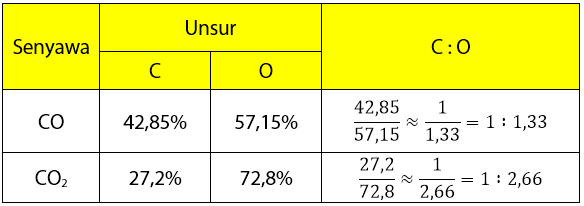
Perbandingan massa oksigen dalam CO2 dan CO = 2,66 : 1,33 = 2 : 1. Perbandingan massa oksigen dalam kedua senyawa adalah bulat sederhana, sesuai dengan hukum Dalton.
Sekian ulasan materi hukum perbandingan berganda atau yang juga disebut sebagai hukum dalton yang meliputi bunyi hukum perbandingan berganda dan contoh soal dengan pembahasannya. Terima kasih sudah mengunjungi idschool(dot)net, semoga bermanfaat.
Baca Juga: 6 Macam Ikatan Kovalen
